


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 2023-09-23
التاريخ: 2023-09-12
التاريخ: 16-2-2016
التاريخ: 2023-12-03
|
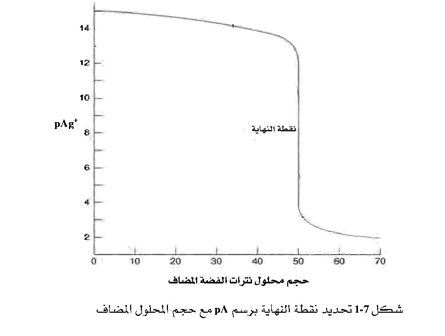
تعتمد هذه الطريقة على التغير في تركيز المادة المقاسة( Analyte) بعد كل إضافة من المادة المقايسة (Titrant)، وكما هو معلوم فإن التغيرات في تركيز المادة المقاسة في بدء العملية ونهايتها تكون قليلة، ولكن عند الاقتراب من نقطة النهاية فإن هذه التغيرات تزداد بشكل ملحوظ، مما يساعد على تحديد نقطة النهاية، ويبلغ التغير في التركيز أقصى قيمة له عند نقطة التكافؤ، النقطة وهي التي عندها يكون عدد مولات المادة المقاسة مكافئاً تماماً لعدد مولات المادة المقايسة وعندها يكون التفاعل قد انتهى (Completed).
وحيث إن التراكيز تتغير في مدى واسع وعند رسم تركيز المادة المقاسة مقابل الحجم المضاف من المادة المقايسة (Titrant)، فإننا لن نحصل على نقطة النهاية بشكل واضح، حيث إن التغير في التركيز عند نقطة النهاية لن يكون واضحاً. ولكن إذا ما تم رسم [log [A - =pA حيث A تدل على المادة المقاسة (Analyte) مقابل الحجم المضاف من المادة المقايسة (Titrant) فسينتج منحنى معايرة يمكن منه بسهوله تحديد نقطة النهاية. فنقطة النهاية هي . النقطة التي عندها يغير المنحنى اتجاهه. وبعد تحديد هذه النقطة ينزل منها عمود على المحور السيني لتحديد حجم المادة المقايسة. ومن العلاقة V1C1=V2C2حيث V1 تمثل حجم المادة المقايسة، C1 تركيز هذه المادة V2 يمثل حجم المادة المقاسة المأخوذ ، C2 هي عبارة عن تركيز المادة في العينة المجهولة. هذا ويجب استخدام المعادلة الموزونة وأخذ المعاملات الناتجة واستخدامها في العلاقة السابقة ليكون عدد المولات من المادة المقاسة مكافئاً لعدد المولات من المادة المقايسة اللازمة لإنهاء التفاعل.
والشكل التالي يبين منحنى معايرة محلول الأيوديد مع محلول نترات الفضة وكيف يمكن معرفة نقطة النهاية من هذا المنحنى


|
|
|
|
علامات بسيطة في جسدك قد تنذر بمرض "قاتل"
|
|
|
|
|
|
|
أول صور ثلاثية الأبعاد للغدة الزعترية البشرية
|
|
|
|
|
|
|
مكتبة أمّ البنين النسويّة تصدر العدد 212 من مجلّة رياض الزهراء (عليها السلام)
|
|
|