
آخر المواضيع المضافة


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
أقرأ أيضاً
التاريخ: 2024-02-07
التاريخ: 17-4-2017
التاريخ: 31-7-2020
التاريخ: 16-4-2017
|
في تفاعلات الترسيب هذه يستخدم محلول قياسي لنترات الفضة ومنحني المعايرة تفاعلات الترسيب يشبه تماماً محنيات المعايرة في تفاعلات التعادل ويمكن أن يرسم المنحني من pCl = -Log Cl-)) وحجم نترات الفضة المضافة .
نفترض أننا نعاير 100 مل من محلول 0.1 عياري كلوريد الصوديوم بمحلول0.1 عياري نترات الفضة
أ ) قبل بدء المعايرة :

ب ) أثناء المعايرة وقبل نقطة التكافؤ :
عند إضافة 10 مل من نترات الفضة
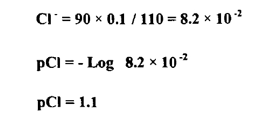
عند إضافة 50 مل من نترات الفضة :

عند إضافة 90 مل من نترات الفضة :

عند إضافة 99.8مل من نترات الفضة :
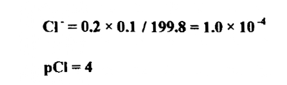
ج ) أثناء المعايرة وقبل نقطة التكافؤ :
عند إضافة 100 مل من نترات الفضة 0.1 عياري إلي 100 مل من كلوريد الصوديوم 0.1 عياري يتكون محلول مشبع من كلوريد الفضة حيث يكون :

د) بعد نقطة التكافؤ :



|
|
|
|
التوتر والسرطان.. علماء يحذرون من "صلة خطيرة"
|
|
|
|
|
|
|
مرآة السيارة: مدى دقة عكسها للصورة الصحيحة
|
|
|
|
|
|
|
نحو شراكة وطنية متكاملة.. الأمين العام للعتبة الحسينية يبحث مع وكيل وزارة الخارجية آفاق التعاون المؤسسي
|
|
|