


 علم الكيمياء
علم الكيمياء 
 الكيمياء التحليلية
الكيمياء التحليلية 
 الكيمياء الحياتية
الكيمياء الحياتية 
 الكيمياء العضوية
الكيمياء العضوية 
 الكيمياء الفيزيائية
الكيمياء الفيزيائية
 الكيمياء اللاعضوية
الكيمياء اللاعضوية 
 مواضيع اخرى في الكيمياء
مواضيع اخرى في الكيمياء
 الكيمياء الصناعية
الكيمياء الصناعية |
Read More
Date: 14-11-2019
Date: 23-10-2019
Date: 20-12-2015
|
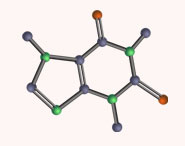
A more detailed model of covalent bonding requires a consideration of valence shell atomic orbitals. For second period elements such as carbon, nitrogen and oxygen, these orbitals have been designated 2s, 2px, 2py & 2pz The spatial distribution of electrons occupying each of these orbitals is shown in the diagram below.

The valence shell electron configuration of carbon is 2s2, 2px1, 2py1 & 2pz0. If this were the configuration used in covalent bonding, carbon would only be able to form two bonds. In this case, the valence shell would have six electrons- two shy of an octet. However, the tetrahedral structures of methane and carbon tetrachloride demonstrate that carbon can form four equivalent bonds, leading to the desired octet. In order to explain this covalent bonding, Linus Pauling proposed an orbital hybridization model in which all the valence shell electrons of carbon are reorganized.


|
|
|
|
حمية العقل.. نظام صحي لإطالة شباب دماغك
|
|
|
|
|
|
|
إيرباص تكشف عن نموذج تجريبي من نصف طائرة ونصف هليكوبتر
|
|
|
|
|
|
اختتام الأسبوع الثاني من الشهر الثالث للبرنامج المركزي لمنتسبي العتبة العباسية
|
|
|
|
راية قبة مرقد أبي الفضل العباس (عليه السلام) تتوسط جناح العتبة العباسية في معرض طهران
|
|
|
|
جامعة العميد وقسم الشؤون الفكرية يعقدان شراكة علمية حول مجلة (تسليم)
|
|
|
|
قسم الشؤون الفكريّة يفتتح باب التسجيل في دورات المواهب
|