

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
الاحلال بالمذيب . الدعم النوكليوفيلي للمذيب
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 288 - 6th ed
5-3-2017
3545
الاحلال بالمذيب . الدعم النوكليوفيلي للمذيب
Solvolysis Nucleophilic assistance by the solvent
ان الاستبدال النوكليوفيلي الاليفاتي في اوجهه المختلفة كان لسنوات طويلة الاكثر دراسة – من الاكثر الأمور جدلاً – في مجال الكيمياء العضوية. لقد كانت السمة الأكثر اهمية في الدراسة – والأكثر جدلاً – مركزة على الحالة الخاصة التي يكون فيها المذيب نوكليوفيلاً: الحلحلة.

ليس هنالك إضافة لنوكليوفيل قوي، ولذلك تقع الحلحلة من اجل ركائز كثيرة في الفئة التي تعدى SN1 . وهذا يعني ان التفاعل يجري وفق خطوتين او اكثر مع تشكل مركب متوسط هو كاتيون عضوي. إن هذا المركب المتوسط هو لب المشكلة: طبيعته ، كيف يتشكل وكيف يتفاعل. وعند دراستنا للحلحلة فإننا ندرس جميع التفاعلات SN1 ، وبطرق عدة، وكل التفاعلات التي تتضمن كربوكاتيونات متوسطة.
من المحتمل ان يكون السؤال الأكبر الذي يتطلب الإجابة عليه هو: ما هو الدور الذي يلعبه المذيب تماماً ؟ من جهة فقط يقوم ببساطة بالتجمع حول الكربوكاتيون والانيون – والحالة الانتقالية تقود إلى تشكلهما – وهكذا يساعد في التحلل اللامتجانس عن طريق تشكل روابط ايون ثنائي قطب؟ أو من جهة اخرى هل يقوم جزيء مذيب مفرد بدور النوكليوفيل فيساعد على دفع الزمرة المغادرة خارج الجزيء؟ (انظر الشكل 1.1) لا يمكن استخدام الحركة هنا لإعطاء جواب مباشر مع العلم ان المذيب لا يتغير خلال مسيرة التفاعل.
يبدو من الواضح ان المذيب يستطيع ان يقدم دعماً نوكليوفيلياً للمنظومة . وتعتمد قوة هذا الدعم على:
(أ) القوة النوكليوفيلية للمذيب.
(ب) مدى الحاجة إلى الدعم.
(جـ) الحدث الذي يكون فيه الكربون متاحاً فراغياً للجزيء الذي هو بحاجة إلى الدعم.
فمثلاً ، يعد الماء والميتانول والايتانول نوكليوفيلات قوية عند استخدامها مذيبات. اي ان حمض الاسيتيك (CH3COOH) أضعف وحمض الفورميك (HCOOH) أكثر ضعفاً. وتكون المذيبات ثلاثي فلورو حمض الاسيتيك (CF3COOH) والكحول ثلاثي فلورو الاثيل (CF3CH2OH) والكحول سداسي فلورو الايزوبروبيل (CF3CHOHCF3) ضعيفة جداً، نسحب ذرات الفلور ذات الكهرسلبية العالية الالكترونات بقوة من الاكسجين ، وبالتالي تخفض من أساسيتها ومن قوتها النوكليوقيلية.
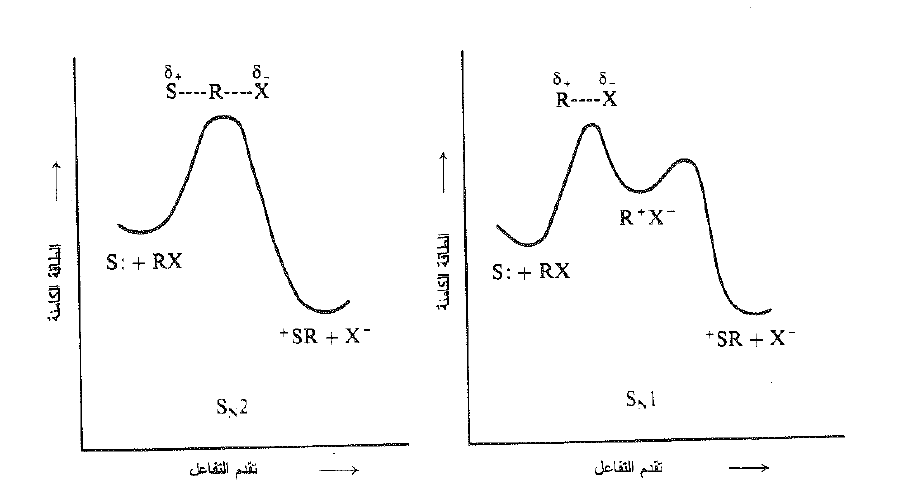
الشكل 1.1: تغيرات الطاقة الكامنة عند تقدم التفاعل: الحلحلة وفق الآليتين SN2 و SN1 : يتضمن SN2 خطوة واحدة، مع هجوم نوكليوفيلي على الركيزة من قبل المذيب ليعطي المنتج مباشرة. تتضمن الحلحلة SN1 خطوتين (او أكثر) بدون هجوم نوكليوفيلي من المذيب على الركيزة ، ويكون المركب المتوسط كربوكاتيوناً.
لقد وجد ان تفاعلية الركائز الثالثية تعتمد على القوة النوكليوفيلي للمذيب وبشكل رئيس على قوتها التأينية .
يكون تشكل الكاتيون الثالثي سهلاً نسبياً يحتاج إلى دعم نوكليوفيلي قليل، وعلى كل حال، يعيق الازدحام مثل هذا الدعم. وتعتمد تفاعلية الركائز الثانوية على كل من القوة النوكليوفيلية والقوة التأينية للمذيب، ويكون تشكل الكاتيونات الثانوية اكثر صعوبة ويحتاج إلى دعم نوكليوفيلي. ومن المحتمل ان يكون التفاعل من النوع SN2 وبشكل مباشر في معظم الركائز الأولية. خطوة وحيدة ويقوم المذيب بدور النوكليوفيل.
لنركز الآن على ركائز الألكيل الثانوية. ماذا تعني بعبارة الدعم النوكليوفيلي على وجه التحديد ؟ قبل كل شيء يختلف هذا الدعم عن نوع الهجوم SN2، بما يلي: إنه يؤدي إلى تشكل كاتيون متوسط وليس المنتج. وكذلك يختلف عن التذوب Solvation العام بأنه يتضمن جزئياً واحداً من المذيب، وليس مجموعة من الجزيئات المتعنقدة . تهاجم الطرف الامامي. ويتشكل عندئذ الكربوكاتيون – أو على الأغلب شيء ما له الكثير من صفات الكربوكاتيون – ويلصق جزيء من المذيب إلى طرفه الخلفي والزمرة المغادرة إلى طرفه الامامي.

وقد يكون كل منهما مرتبطاً إلى الكربون عن طريق تراكب انتفاخ لحد المدارات P للكربون – المدار P الفارغ في الكربوكاتيون التقليدي. وتكون الهندسة مشابهة للحالة الانتقالية في التفاعل SN2 ولكنها مركب متوسط وتتوافق مع الطاقة الدنيا في منحني تقدم التفاعل. إذا كانت الزمرة المغادرة انيوناً، وكان المذيب ذا قطبية معتدلة، فإن الارتباط بين الكاتيون والانيون يكون في معظمه ربطاً كهرساكناً ، ويكون الكلام عن زوجين انيونيين (على الرغم من ان جزيء مذيب واحد يلعب دوراً خاصاً هنا، وبالطبع تتعقد جزيئات المذيب الأخرى حول الايونات وتؤدي دورها المعتاد ).
يتفاعل الآن هذا المركب المتوسط الكاتيوني مع هذا الكربوكاتيون النوكليوفيلي المذوب. يفتح امامه مجالاً واسعاً من التفاعلات التي يمكن ان تقوم بها الكربوكاتيونات. ففي التفاعل الذي نهتم به هنا، تتحدد مع جزيء المذيب – مع تشكل رابطة كاملة – لتعطي المنتج. وإذا كانت الزمرة المغادرة في وقت حدود التفاعل مع المذيب يحدث من الجهة الخلفية. ومن ناحية اخرى، إذا استمر الكاتيون فترة طويلة تكفي لاستبدال جزيء مذيب آخر بالزمرة المغادرة، فإنه يتشكل مركب متوسط متناظر، ويكون من المحتمل ان يحدث هذا التفاعل من الإمام ومن الخلف. لذلك، يمكن ان يحدث التذوب مع انقلاب كامل او مع انقلاب مضاف إليه مقادير مختلفة من الرسمزة.
كشف العمل الممتاز الذي قام به سابول ونستين Saul Winstein (جامعة كاليفورينيا – لوس انجلوس) عن السلوك المفصل للألكترونين الايونيين اللذين يعدان مركبان متوسطة في بعض حالات الحلحلة: الزوجان الايونيان الوثيقا الارتباط (ذوا ألفة شديدة)، حيث يكون الكاتيون التابع لهما حراً بشكل يكفي ليدور حول نفسه ويفقد التشكيل ، ومع ذلك يكون مرتبطاً بإحكام بحيث تكون إعادة الاتحاد مع المركب المرتبط برابطة مشتركة مفضلاً الزوجين الايونيين القليلي الارتباط (المفصولة بالمذيب) ويكون الكاتيون التابع لهما عرضة لهجوم النوكليوفيلات الخارجية.
ثمة اقتراح يقوا ان هنالك طيفاً مستمراً من الآليات للحلحلة تمتد من التفاعل SN1 التقليدي من جهة إلى تفاعل الخطوة الواحدة SN2 من الجهة الأخرى. ويتضح من منحنيات تقدم التفاعل ان النهاية الدنيا لطاقة الكربوكاتيون تصبح اقل عمقاً عندما نبتعد عن الجهة SN1، وتختفي النهاية عند الطرف SN2 حيث نحصل على نهاية عظمى وحيدة.
وفيما بين نهايتي الطيف، تقع الآليات المتضمنة درجات متفاوتة من الدعم النوكليوفيلي للمذيب. واطلق بول سكلير Paul Schleyer ، الذي صورته للدعم النوكليوفيلي مماثلة لما وصفناه سابقاً، على هذه الآليات اسم "الآليات SN2 المتوسطة" ، أي التفاعلات SN2 المتضمنة تشكل مركب متوسط، تملك مثل هذه الآلية صفات كل من الآليات التقليدية ، والتفاعل SN2 الوحيد الخطوة و SN1 . ويؤكد مصطلح سكلير على المفهوم SN2، أي الهجوم النوكليوفيلي تصبح جزءاً من القوة المحركة للتفاعل.
على كل حال، في هذا الكتاب، سنعالج الآلية على أنها تعديل للآلية SN1. هنالك مركب متوسط كاتيوني متشكل من مركب قادر على فعل كل ما يمكن ان يفعله الكربوكاتيون – كما ان تشتت الشحنة الموجبة الناشئة تقدم مقداراً كبيراً من القوة المحركة للتفاعل ، سوف ندجل على مثل هذا التفاعل على انه يتبع الآلية SN1 مع دعم نوكليوفيلي من المذيب، وسوف ندعو المركب المتوسط الكربوكاتيون النوكليوفيلي المذوب. وفي بعض الاحيان الكربوكاتيون المعاق.
ان المصطلح الدقيق الذي نستخدمه ليس مهماً ما دمنا نفهم بعضنا بعضاً. أما المفهم فهو ان نرى عمل نفس العوامل الاساسية التي عرفها من قبل هيوز وانكولد Hughes ans Ingold منذ خمسين سنة مضت: هجوم نوكليوفيلي يخضع للأعاقة الفراغية، وتشتت للشحنة بالمتبادلات وبالمذيب، والجديد فهو فعمنا المتزايد لمقدار اهمية كل ممن هذين العاملين.
يجب ان نحتفظ بإحساسنا التأملي هنا، إذ أننا نناقش الحالة الخاصة، الحلحلة، ومعظم ما قلناه يتعلق فقط بركائز الالكيل الثانوية . إن الفروق في الاستقرار بين الانواع المختلفة من الكربوكاتيونات كبير إلى حد يجعل التفاعلات قابلة المتصنيف في ثلاثة مجموعات منفصلة : (أ) التفاعل SN2 ذو الخطوة الوحيدة من اجل الركائز الأولى ، (ب) التفاعل SN1 مع مركب متوسط يقرب فكرتنا بشأن الكربوكاتيون البسيط (المذوب) من اجل الركائز الثالثية ، (جـ) تفاعل ذو خطوتين من اجل الركائز الثانوية يشبه التفاعل SN1 من حيث وجود مركب كاتيوني متوسط ولكنه يتشكل بدعم نوكليوفيلي مع بقاء الاعاقة من النوكليوفيل (المذيب) والزمرة المغادرة. ان الدعم النوكليوفيلي عامل مهم في شرح التفاعليات النسبية في الركائز الثانوية وتفاعلياتها في مذيبات مختلفة، ولكن عندما يكون الدعم النوكليوفيلي غير قوي فإن عامل تشتت الشحنة هو الذي يدفع الركائز التالية للتفاعل – بدون اي دعم نوكليوفيلي – بسرعة اكبر من الركائز الثانوية.
 الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
الاكثر قراءة في مواضيع عامة في الكيمياء العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















