

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
الخواص الفيزيائية Physical properties
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 99 - 6th ed
22-11-2016
12824
الخواص الفيزيائية Physical properties
تتعلف الخواص الفيزيائية للألكانات، التي تلي الميتان، ببنية الألكان. ترتبط الذرات في جزيء الألكان بروابط مشتركة فإما أن تصل هذه الروابط ذرتين من النوع نفسه وعليه فهي لا قطبية، أو أن تصل ذرتين تختلفان عن بعضهما قليلاً جداً بالكهرسلبية، وعليه فهي قليلة القطبية. زد على ذلك، أن هذه الروابط تكون موجهة بشكل متناظر جداً، الأمر الذي يؤدي الى ميل هذه القطبيات الرابطية الى افناء بعضها بعضاً. والنتيجة هي أن جزيء الألكان إما أن يكون ضعيف القطبية جداً أو أن يكون لا قطبياً.
رأينا أن القوى التي تمسك الجزيئات اللاقطبية الى بعضها بعضا (قوى فاندرفالس) تكون ضعيفة وذات تأثير قصير المدى جداً؛ وهي تعمل فقط بين أجزاء من الجزيئات المختلفة، التي تكون في تماس قريب معها أي بين سطوح الجزيئات. لذلك يمكننا أن نتوقع داخل الطائفة الواحدة أن تكون القوى بين الجزيئات الكبيرة ذات السطوح الكبيرة هي الأقوى.
يتضمن الجدول 3.3 بعض الثوابت الفيزيائية لعدد من الألكانات. ونستطيع أن نرى أن نقاط الغليان والانصهار تزداد بازدياد عدد ذرات الكربون.
تتطلب عملية الغليان أو الانصهار، التغلب على القوى ما بين الجزيئية في سائل أو صلب وتزداد نقاط الغليان أو الانصهار لأن القوى ما بين الجزيئية هذه تزداد كلما أصبحت الجزيئات المعنية أكبر.
تزداد نقطة الغليان، ما عدا ما يتعلق بالألكانات الصغيرة جداً، من 20˚س الى 30˚س من أجل كل كربون يضاف الى السلسلة وسوف نرى أن هذه الزيادة (20˚س – 30˚س) لكل كربون، لا تخص الألكانات فقط، بل كلاً من سلاسل الأقران التي سندرسها أيضاً.
ليست الزيادة في نقطة الانصهار منتظمة تماماً لأن القوى ما بين الجزيئية في البلورة لا تتعلق فقط بحجم الجزيئات، بل بكيفية انتظامها في الشبكة البلورية أيضاً.
إن الألكانات الأربعة الأولى غازات، ونتيجة لارتفاع نقطة الغليان والانصهار بازدياد طول السلسلة، تكون الألكانات الثلاثة عشر التالية (C17-C5) سوائل، أما الألكانات التي تحوي (18) كربون أو أكثر فتكون صلبة.
الجدول 3.3: الألكانات
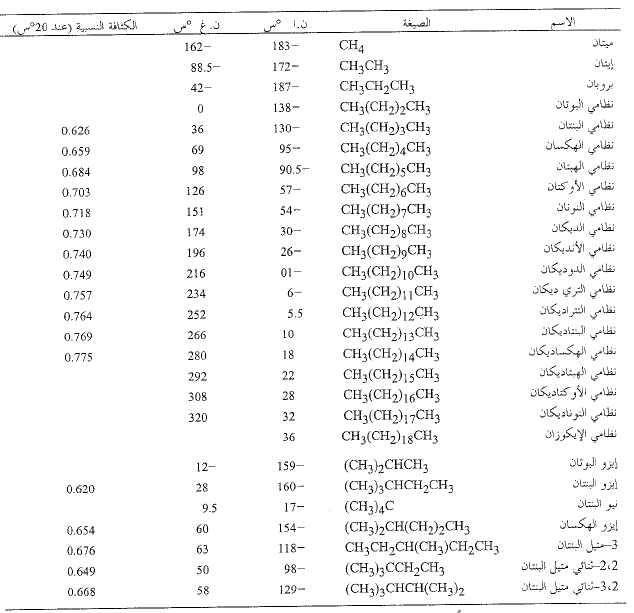
توجد اختلافات صغيرة نوعاً ما في نقاط غليان الألكانات التي لها العدد نفسه من ذرات الكربون إلا أن لها بُنى مختلفة. أعطيت نقاط غليان مماكبات البوتان والبنتان والهكسان في الفقرتين (4.3 – 6.3). نلاحظ من ذلك أنه في كل حالة تكون نقطة غليان المماكب ذي السلسلة المتفرعة، أدنى من تلك التي للماكب ذي السلسلة غير المتفرعة، وهكذا كلما ازداد عدد الفروع كلما انخفضت نقطة الغليان. وعليه، تكون نقطة غليان نظامي البوتان 0˚س، وتكون 12˚س لإيزو البوتان و 36˚س لنظامي البنتان و28˚س لإيزو البنتان مع تفرع واحد، و9.5˚س لنيوالبنتان مع تفرعين.
وقد لوحظ تأثيرات التفرع هذا على نقاط الغليان في جميع طوائف المركبات العضوية. يمكن فهم خفض التفرع لنقطة الغليان كما يلي: يميل شكل الجزيء بالتفرع الى الاقتراب من شكل الكرة؛ وعندما يحدث هذا تتناقص مساحة السطح مما يؤدي الى جعل القوى ما بين الجزيئات أضعف ويصبح التغلب عليها ممكن في درجات حرارة أقل.
قارن أشكال مماكبات البنتان، مثلاً، كما هي مبينة في الشكل 1.1. وبالتوافق مع قاعدة (البصمة): (الشبيه يذيب شبيهه) فإن الألكانات تذوب في مذيبات لا قطبية مثل البنزين والإيثر والكلوروفورم ولا تذوب في الماء أو في مُحلات أخرى أكثر قطبية. وبالمثل لدى اعتبار الألكانات بمثابة مذيبات، تذيب المركبات ذات القطبية المنخفضة ولا تذيب المركبات ذات القطبية العالية.
تزداد الكثافة النسبية مع حجم الألكان، إلا أنها تميل الى الاستواء عند قيمة للكثافة تساوي (0.8)؛ وهكذا تكون جميع الألكانات أقل كثافة من الماء.
وليس مستغرباً أن تكون جميع المركبات العضوية، تقريباً، أقل كثافة من الماء، طالما أنها تحوي الكربون والهيدروجين، بشكل رئيسي. وعموماً لكي يكون مركب ما أكثف من الماء، عليه أن يحوي ذرة ثقيلة كالبروم أو اليود، أو عدداً من الذرات مثل الكلور.
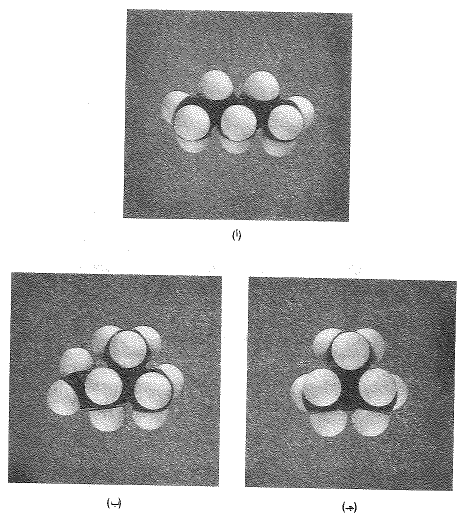
الشكل 1.1: البنية الجزيئية والخواص الفيزيائية: تأثير التفرع. مماكبات البنتان: (أ) نظامي البنتان، نقطة الغليان 36˚س، (ب) إيزو البنتان، نقطة الغليان 28˚س، (جـ) نيو البنتان، نقطة الغليان 9.5˚س. إن نيو البنتان هو الأكثر تفرعاً والأكثر كروية، تقريباً، وهو يملك مساحة السطح الأصغرية؛ وتكون القوى ما بين الجزيئية أضعف، ولذلك يغلي في الدرجة الأخفض.
 الاكثر قراءة في الهايدروكاربونات
الاكثر قراءة في الهايدروكاربونات
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















