

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
حركية البلمرة التكثيفية Kinetic of Condensation Polymerization
المؤلف:
د. عمر بن عبدالله الهزازي
المصدر:
كيمياء البوليمرات
الجزء والصفحة:
ص 209
6-11-2017
947
حركية البلمرة التكثيفية Kinetic of Condensation Polymerization
يلاحظ في البلمرة التكثيفية ان المونومير يختفي منذ المراحل الأولى من التفاعل، فعندما تصل جزيئات البوليمر إلى عشر وحدات بنائية متكررة لا تتعدى نسبة المونومير في مزيد التفاعل عن (1 %) . من ناحية اخرى نجد في البلمرة التكثيفية إمكانية حدوث التفاعل البلمرة التكثيفية تتمثل بمجموعة سرع التفاعلات المختلفة التي تحدث بين الجزيئات المتباينة الحجوم، ولقد أثبتت التجارب العلمية بعض الحقائق التي تتلخص فيما يلي:
1) إن فعالية المجموعتين الدالتين في جزيئات المونوميرات متكافئة في فعالية البلمرة إذا كانتا مفصولتين عن بعضهما بأكثر من ذرتي كربون.
2) ان فعالية اي من المجاميع الدالة لا تعتمد على طبيعة المجموعة الدالة الاخرى في الجزيئة سواء كانت متفاعلة او غير متفاعلة.
3) ان فعالية المجاميع الدالة لا تعتمد على حجم الجزيئة.
ولبيان حركية البلمرة التكثيفية نأخذ تحضير البولي استرات كمثال لهذا النوع من التفاعل. من المعروف بأن الاسترة البسيطة تتم عادة بوجود عوامل مساعدة حامضية حيث يتم التفاعل على خطوتين أساسيتين هما: خطوة إضافة البروتون إلى مجموعة الكاربونيل في الحامض الكربوكسيلي ، وخطوة تفاعل الكحول مع مجموعة الحامض المضاف إليها البروتون ، كما هو موضح في المعادلات الآتية:
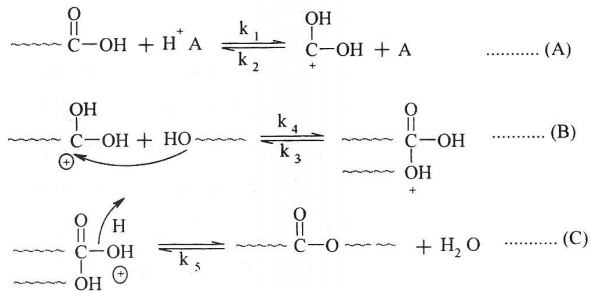
ويقصد بــ (الخطوط المتعرجة) كافة الجزيئات التي تحمل المجاميع الفعالة الدالة. ان طبيعة معظم تفاعلات التكثيف بشكل عام وتفاعلات الاسترة (esterfication) بشكل خاص هي من التفاعلات العكسية وتنتهي بالاتزان (equilibrium) ، وللحصول على بوليمر ذو وزن جزيئي عالي يستوجب ان يسير التفاعل باتجاه واحد وهو اتجاه تكوين البوليمر. لذا يجب ازالة الناتج الثانوي المتكون في تفاعل البلمرة وبذلك يستمر التفاعل نحو تكوين البوليمر، وعند ذلك يمكننا اعتبار التفاعل غير عكسي عند دراسة حركية التفاعل في مثل هذه الظروف الخاصة.
يعبر عادة عن سرعة تفاعل البلمرة بدلالة تراكيز المجاميع الدالة المتفاعلة، ويمكن تتبع سير التفاعل عملياً وذلك بمعايرة مزيج التفاعل مع قاعدة لغرض تعيين تركيز مجاميع الكربوكسيل المتبقية بعد مرور فترات زمنية مختلفة منذ بدء البلمرة.
ولقد وجد في تفاعلات تكوين البولي استرات ان خطوة إضافة البروتون إلى مجموعة الكربوكسيل تعد بمثابة الخطوة المحددة لسرعة تفاعل البلمرة ويمكن التعبير عن سرعة التفاعل لمرحلة التكاثر من المعادلة:
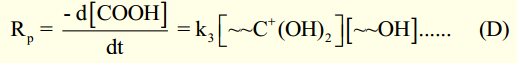
حيث أن K3[∽∽C+(OH)2][∽∽OH] تمثل تراكيز مجاميع الكربوكسيل والهيدروكسيل والكربوكسيل المتحد ببروتون على التوالي مقاسة بوحدات المول /لتر . وهذه المعادلة غير مستعملة عملياً لتعيين سرعة تفاعل البلمرة لأنه لا يمكن إيجاد تركيز
[C+(OH)2] بسهوله، لذلك يحول إلى صيغة أكثر عملية وذلك بالتعويض عن تركيز [C+(OH)2]في المعادلة المتوازنة (A) بما يساويها كما يلي:
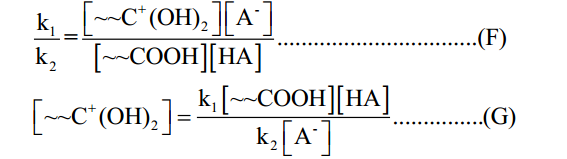
وبالتعويض عن قيمة [C+(OH)2] في المعادلة D نحصل على:
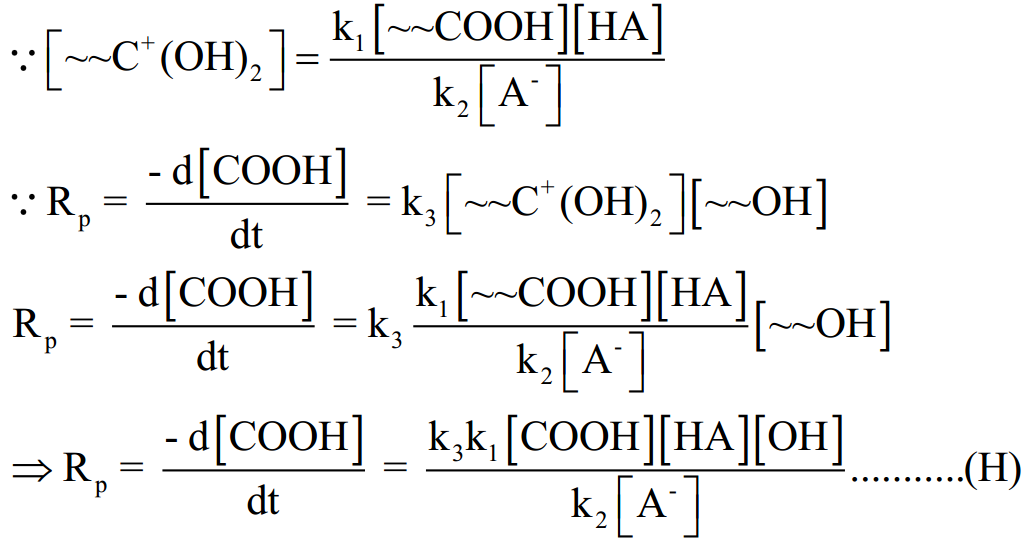
يمكن التعبير عن قيمة [A-] تركيب الشق السالب للحامض من معادلة تفكك الحامض الآتية:

وبالتعويض عن قيمة [A-] تركيز الشق السالب للحامض من معادلة تفكك الحامض (معادلة J) نحصل على:

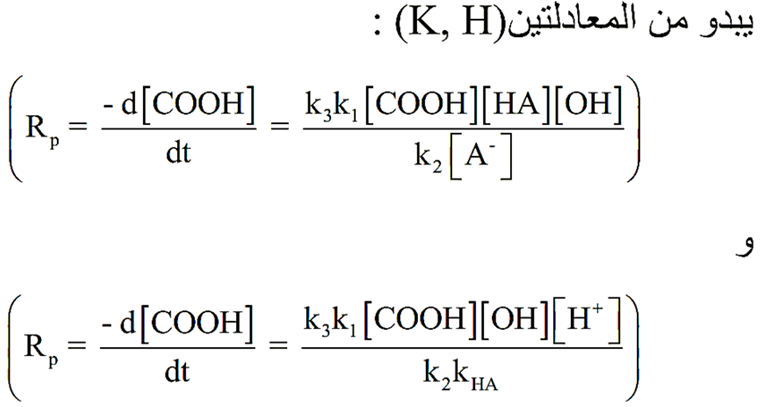
ان لطبيعة الحامض المستخدم تأثير كبير على سرعة البلمرة فيما إذا كان الحامض المستعمل حامضاً قوياً مثل حامض الكبريتيك الذي يستخدم كعامل مساعد خارجي او في حالة عدم استخدام حامض كعامل مساعد خارجي
 الاكثر قراءة في كيمياء البوليمرات
الاكثر قراءة في كيمياء البوليمرات
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















