

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
SN2 مقابل SN1vs.SN2 : SN1
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 223- 6th ed
15-2-2017
3262
SN2 مقابل SN1:SN2 vs. SN1
وصفنا فيما مضى آليتين للتبادل النوكليوفيلي: الآلية SN2، والتي تنمو:
(أ) بحركية من المرتبة الثانية.
(ب) بانقلاب تام للراغية الكيميائية.
(ج) بغياب إعادة الترتيب.
(د) بترتيب للتفاعلية هو 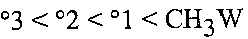
والآلية SN1 التي تتميز:
(أ) بحركية من المرتبة الأولى
(ب) برسمزة.
(جـ) بوجود إعادة ترتيب.
(د) بترتيب للتفاعلية هو 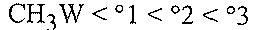
ناقشتا هاتين الآليتين منفصلتين عن بعضهما. ولنعد الآن إلى العلاقة بين الآليتين. فمن أجل ركيزة معينة وفي شروط معطاة، أي الآليتين سيتبعها التفاعل؟ وماذا نستطيع أن نفعل، إن اسمكن، لتوجيه تفاعل نحو إحداهما أو نحو الأخرى؟
للإجابة عن هذه الأسئلة، لندرس فقط ما يمكن أن يحدث لجزيء الركيزة. يمكنه أن عاني هجوماً نوكليوفيلياً من الجهة الخلفية، أو ان يعاني تحللاً لا متجانساً مكوناً كربوكاتيوناً. والعملية التي تحدث بشكل أسرع، تعين الآلية المسيطرة. (نذكر ان التحلل اللامتجانس هو الخطوة الأولى والمعينة للسرعة وفق الآلية SN1).

مرة أخرى، يجب علينا ان نعود إلى موضوع السرع النسبية لتفاعلات متنافسة.
لنتفحص كل مكون من المنظومة التفاعلية، ثم لنر التأثير يمارس على هذا التنافس بين الهجوم النوكليوفيلي والتحلل اللامتجانس.
لنبدأ بالركيزة، المكونة من قسمين : زمرة الألكيل والزمرة المغادرة. والطبع، فغن طبيعة الزمرة المغادرة، أمر حيوي بالنسبة لحدوث الاستبدال ، ومهما يكن نوع العملية التي تحدث ، هجوماً نوكليوفيلياً كانت أم تحللاً لا متجانساً، فإن الرابطة مع الزمرة المغادرة ستتكسر، وكلما كان كسر الرابطة أسرع، أي كلما كانت الزمرة المغادرة أكثر جودة، كلما كان التفاعل أسرع حدوثاً. وهكذا تسرع الزمرة الجيدة الرحيل، التفاعل وفق الآليتين كلتيهما وكما يحدث فعلاً فهي نسرع الآنيتين بالدرجة نفسها. وبالمحصلة يكون لطبيعة الزمرة المغادرة تأثير صغير بما يخص أبا من الآليتين تكون مسيطرة SN2 أو SN1.
وعلى العكس ، فإن طبيعة زمرة الألكيل (R) في الركيزة، تمارس تأثيراً عميقاً على اي من الآليتين يجري وفقها التفاعل. يوجد في الزمرة (R) عاملان بنيويان فاعلان هما المنع الفراغي الذي يعين سهولة الهجوم من الجهة الخلقية، والقدرة على احتضان الشحنة الموجبة، التي تعين بدرجة كبيرة سهولة التحلل للامتجانس. وكلما تقدمنا على طول السلسلة ,CH3,1o,2o,3o تغدو الزمرة (R) بالتعريف أكثر تفرعاً . أي ان هنالك تزايداً في عدد المبادلات على الكربون، وهي مبادلات كبيرة الحجم ومائحة للألكرتونات. يزداد المنع الفراغي، ويغدو الهجوم من الجهة الخلفية أكثر صعوبة، وعليه فهو يغدو أكثر بطا. وتزداد في الوقت نفسه قابلية احتضان الشحنة الموجبة، وهكذا فإن التحليل اللامتجانس يغدو أكثر سهولة وبالتالي أكثر سرعة.
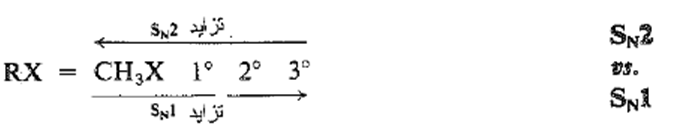
وبالنتيجة يكون لدينا النموذج الذي صادفناه قبلاً : استعداد المتيل والركائز الاولية لاتباع الآلية SN2، واستعداد الركائز الثالثية لأتباع الآلية SN1 . اما الركائز الثانوية فلديها ميل لسلوك متوسط، وهو مزيج من الآليتين ، أو كما سنرى في الفصل السابع، ربما آلية تجمع خواص الآليتين SN2 و SN1 معاً.
وبالرغم من استعداد ركيزة معينة لاتباع آلة معينة، فإنه يبقى بإمكاننا التحكم بمسار التفاعل لدرجة محسوبة باختيار الشروط التجريبية المناسبة. ولكى نرى كيف يتم هذا، علينا نفحص المكونات الأخرى للمنظومة التفاعلية.
لنعد إذن إلى النوكليوفيل. إن الاختلاف الاساسي بين الآليتين SN2 و SN1 هو مسألة متى يشارك النوكليوفيل. إن يشارك في الخطوة المعينة لسرعة SN2 ، ولكنه يشارك بعد الخطوة المعينة لسرعة SN1، يؤدي هذا الفرق في التوقيت مباشرة، إلى عاملين يساعدان في تعيين الآلية المتبعة، وهي تركيز النوكليوفيل وطبيعته.
تتعلق سرعة التفاعل SN2 بتركيز النوكليوفيل، [:Z] الذي هو من المرتبة الثانية.
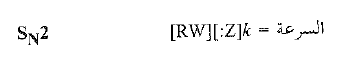
بينما تكون سرعة التفاعل SN1 مستقلة عن تركيز النوكليوفيل [:Z]، وهو من المرتبة الاولى.
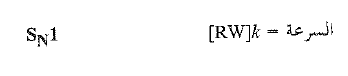
إذن فإن زيادة [:Z] تسرع التفاعل من المرتبة الثانية، إلا أنها لا تؤثر في التفاعل SN1، فيزداد الجزء الخاص بالتفاعل SN2. ويبطئ النقصان في [:Z] التفاعل من المرتبة الثانية، إلا انه لا يؤثر في التفاعل من المرتبة الأولى، فينقص جزء الخاص بالتفاعل SN2 . وتكون المحصلة ، إذا كانت الأمور الأخرى متساوية أن تركيز النوكليوفيل المرتفع يجعل التفاعل وفق SN2 مفضلاً، أما تركيز النوكليوفيل منخفض فيجعل التفاعل SN1 مفضلاً.
وبالطريقة نفسها تتعلق سرعة SN2 بطبيعة النوكليوفيل: يهاجم النوكليوفيل الاقوى ، الركيزة بسرعة . بينما تكون سرعة SN1 مستقلة عن طبيعة النوكليوفيل، وعلى النوكليفيل (ٍسواء كان قوياً أو ضعيفاً) ان ينتظر حتى تكون الكربوكاتيون. وتكون المحصلة، إذا كانت الأمور الأخرى متساوية، ان يجعل النوكليوفيل القوي التفاعل SN2 مفضلاً، بينما يجعل النوكليوفيل الضعيف التفاعل SN1 مفضلاً.
إذ تفاعل بروميد نيو البنتيل مع نوكليوفيل فوي مثل الابتوكسيد مؤدياً إلى منتج غير معاد ترتيبه هو إنيل نيو بنتيل الإيتر، ومن الواضح ان هذا التفاعل هو تفاعل SN2. إنه بتفاعل ، أيضاً، مع نوكليوفيل ضعيف مثل الإيتانول مؤدياً إلى منتج إعادة ترتيب هو إتيل ثالثي بنتيل الايثر. ومن الواضح ان هذا التفاعل هو تفاعل SN1.
إلا أننا أهملنا المكون الثالث في المنظومة التفاعلية وهو المذيب، الذي يقدم السبيل الأفضل للتحكم بالتفاعل. سوف نتفحص دور المذيب، بالتفصيل، في الفصل السابع.
قلنا في بداية هذا الفصل ان التفاعل الكيميائي هو نتيجة للتنافس، والتفاعل الذي يحدث، واقعياً، عندما نخلط مجموعة معينة من المتفاعلات معاً، وفي ظل شروط معينة، هو التفاعل الذي يحدث أسرع. انصب اهتمامنا هنا على التنافس بين السياؤات المختلفة للاستبدال النوكليوفيلي. أما في الفصل الثامن فسنجد انه ما زال هنالك تنافس آخر بين الاستبدال النوكليوفيلي وبين تفاعل من نوع مختلف كلياً، هو الحذف. وقد اهتممنا في كل هذا، بالعوامل التي تجعل آلية واحدة او نوعاً من التفاعلات مفضلة لى الاخرى، واهتممنا كذلك بما نستطيع فعله للتحكم بمحصلة التفاعل.
 الاكثر قراءة في المركبات الوسطية وميكانيكيات التفاعلات العضوية
الاكثر قراءة في المركبات الوسطية وميكانيكيات التفاعلات العضوية
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















