

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء التناسقية

الكيمياء الاشعاعية والنووية
الماء السائل مذيبا(Liquid water as a solvent)
المؤلف:
غاري و. فان لون , ستيفن ج. دفي
المصدر:
كيمياء البيئة نظرة شاملة
الجزء والصفحة:
ص376 -377
2023-12-27
1863
يمتلك الماء قيمتين كبيرتين للعزم الثنائي القطب dipole moment وثابت العزل الكهربائي، وهما من بين أكبر القيم التي تخص السوائل الشائعة وتجعل هاتان الخاصتان الماء مذيباً (solvent) جيداً لكثير من المواد. وفي الواقع، يُسمى الماء أحياناً بالمذيب العام (universal solvent) لأنه يُذيب عدداً من المواد يفوق عدد ما يُذيبه أي سائل آخر تقريباً. وبسبب قيمة العزم الثنائي القطب الكبيرة للماء (Cm -1030 ×6.1 ) ، الوحدة هي كولون متر)، توجه جزيئاته نفسها حول الأجناس المتأينة أو المستقطبة مكونة روابط X...H2O الشكل (6.9). ونظراً إلى أن تلك هي سيرورة طاقة حرة سالبة، يكون تكوين الروابط بغية إنتاج أجناس مُميَّهة hydrated هو التفاعل المفضل. وعندما يكون ربح الطاقة الناجم عن المزج مع الماء أكبر من الطاقة اللازمة لكسر الروابط الأصلية في المادة الصلبة، تكون تلك المادة قابلة للذوبان. إن كثيراً من المواد المتأينة أو المستقطبة سهل الامتزاج بالماء ويوصف بأنه أليف للماء hydrophilic ،
في حين أن المواد غير المستقطبة والمحايدة تتصف بمقدرة محدودة على تكوين روابط مع جزيئات الماء المستقطبة، ولذا توصف بأنها نفورة من الماء hydrophobic.
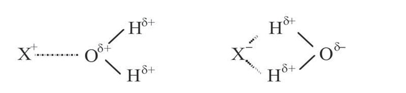
الشكل 6.9: أيونات موجبة وسالبة مُميَّهة. تستطيع الجزيئات المستقطبة أيضاً تكوين أجناس مُميَّهة مشابهة. ويحيط عادة أكثر من جزيء واحد من الماء بالموقع المشحون كهربائياً.
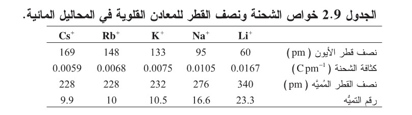
ويعتمد عدد جزيئات الماء التي يمكن أن تحيط بأيون، والذي يُمثل برقم التميُّه، على عدة عوامل أهمها نسبة الشحنة إلى نصف القطر، وفقا للمبيَّن بالبيانات المدرجة في الجدول 2.9 للمعادن القلوية.
تجذب الأيونات، التي تكون فيها نسبة الشحنة إلى نصف القطر كبيرة، أي ذات تركيز الشحنة ،العالي، عدداً أكبر من جزيئات الماء لتحيط بها. وهذا يقود إلى العلاقة العكسية اللافتة بين نصف قطر الأيون ونصف القطر المُميَّه وفقاً للمبين في الجدول 2.9. وهذا ينطوي على مضامين خاصة بمبادلة الأيونات التي تتضمن أيونات مُمَيَّهة والتي تحصل على السطوح الصلبة في عمود الماء. إن نسبة الشحنة إلى نصف القطر في الأيونات المُميَّهة للمعادن القلوية تجعل أيون الربيديوم، مثلاً ، أكثر انجذاباً إلى المواقع السالبة على الأجسام الصلبة، المعلَّقة أو الراسبة، من أيون الصوديوم.
 الاكثر قراءة في كيمياء البيئة
الاكثر قراءة في كيمياء البيئة
 اخر الاخبار
اخر الاخبار
اخبار العتبة العباسية المقدسة

الآخبار الصحية















 قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة
قسم الشؤون الفكرية يصدر كتاباً يوثق تاريخ السدانة في العتبة العباسية المقدسة "المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة
"المهمة".. إصدار قصصي يوثّق القصص الفائزة في مسابقة فتوى الدفاع المقدسة للقصة القصيرة (نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)
(نوافذ).. إصدار أدبي يوثق القصص الفائزة في مسابقة الإمام العسكري (عليه السلام)


















