

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الكيمياء الفراغية لتفاعل E2 . الحذف المناضد syn – والمضاد anti –
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 403
4-4-2017
5548
الكيمياء الفراغية لتفاعل E2 . الحذف المناضد syn – والمضاد anti –
Stereochemistry of the E2 reaction. Syn- and anti - Elimination
لندرس، بعد هذا الكيمياء الفراغية للحذف، مستخدمين مثالاً على ذلك تفاعلاً آخر مألوفاً وهو نزع هالوجين الهيدروجين في شروط E2.
ندرس نزع هالوجين الهيدروجين من هاليد الالكيل، -1 برومو 1-، -2 ثنائي فنيل البروبان. ( تكون زمرة الفنيل C6H5-، وهي زمرة هيدروكربونية عطرية خاملة في شروط التفاعل).
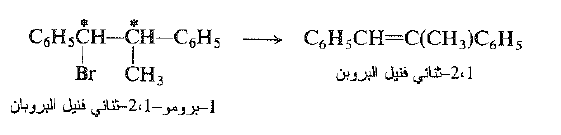
يحوي المركب مركزين كيراليين ، ونستطيع ، بسهولة، إيضاح إمكانية وجوده على شكل شفعين من المتخايلات هما (I)و (II) ، ويسميان بالإرترو erythro و III و IV ويسميان بالتريو threo يكون كل شفع من هذه التشكيلات متماكباً لا متخايلاً مع الشفع الآخر.
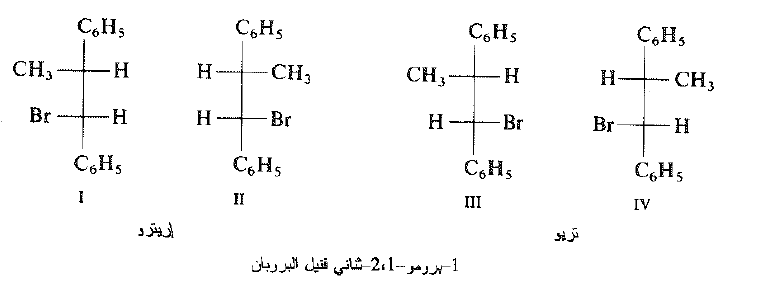
يوجد المنتج أيضاً، على شكل مماكبين فراغيين : شفع من المتماكبان الهندسية (Z) و (E) .
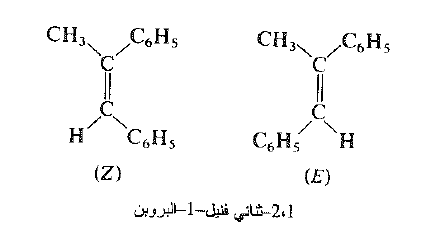
إذا بدأنا الآن بالهاليد "اريتو" ، (I) و (II) ، فإننا نحصل، فقط، على الالكن (Z).
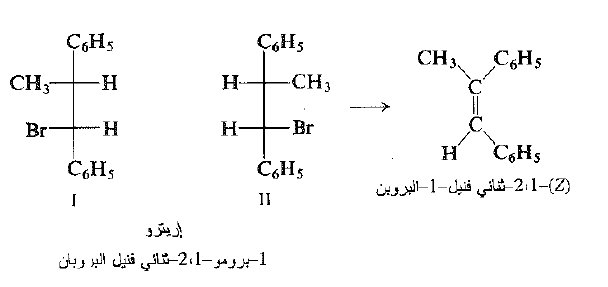
وإذا بدأنا الآن بالهاليد "تريو" ، (III) و (IV) ، فإننا نحصل، فقط، على الالكن (E).
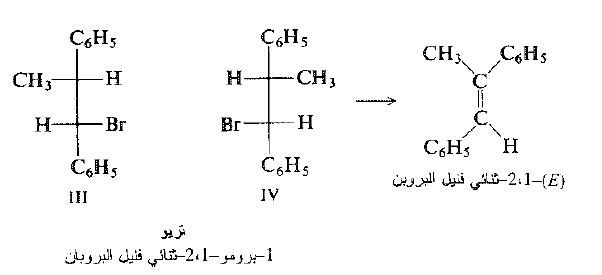
أظهرت دراسات اخرى ان هذه النتائج نموذجية ، فقد أظهرت ان الحذف (E2) انتقائي فراغي ونوعي وفراغي.
ولوصف انواع الانتقائية الفراغية التي يمكن أن نلاحظ في تفاعلات الحذف، نستخدم مفهومي الحذف المناضد والحذف المضاد. ليست هذه التعابير أسماء لآليات نوعية. إنها تشير، ببساطة، إلى حقائق كيميائية فراغية ، أي انه إذا كانت الزمر المحذوفة من الجهة نفسها فالحذف مناضد وإذا كانتا من جهتين متعاكستين ، فالحذف مضاد وذلك بالنسبة للرابطة المزدوجة المتنامية (الشكل 1.1). وكما بين هذا المثال وغيره من الأمثلة العديدة الأخرى، فإن الحذف E2 يتضمن بصورة نموذجية حذفاً مضاداً : فالهيدروجين في الحالة الانتقالية ، وكذلك الزمرة المغادرة ، يوجدان في علاقة مضادة بشكل معاكس لليساري او المخسوف.
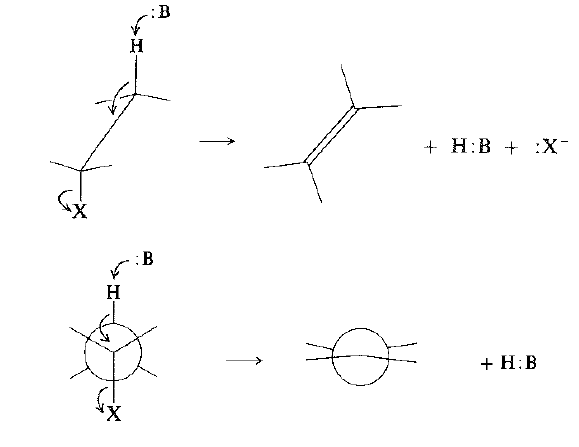
وهكذا، يعطي المماكب اللامتخايل (I) او (متخايله II) الألكن (Z).

الشكل1.1 الحذف "المتضاد" والحذف "المضاد" ويعطي المماكب اللامتخايل (III) أو (متخايله IV) الألكن (E).
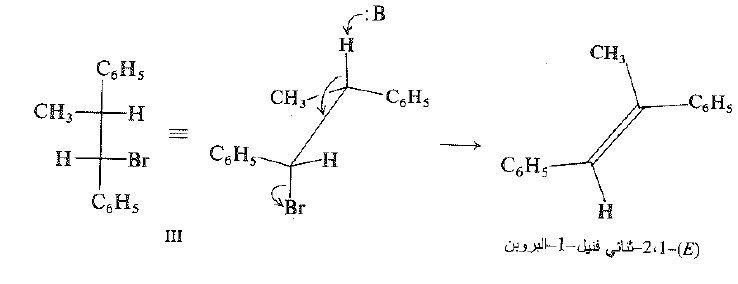
شبهنا سابقاً ( E2) بـ (SN2) حيث يطرد هالوجين خارج الجزيء بنوع من الهجوم النوكليوفيلي حيث يكون النوكليوفيل الكربون B- الذي يستخم الشفع الالكتروني المتبقي بعد رحيل البروتون ، ويقوم بتكوين الرابطة π مع الكربون - α . وعلى هذا الأساس، يشير تفضيل الحذف المضاف إلى انهجوم النوكليوفيل هذا، ويحدث، بشكل مفضل ، على وجه الكربون - α . الأكثر بعداً عن الهالوجين الراحل وهذا الهجوم يشبه الهجوم يشبه الهجوم المألوف من الجهة الخلفية في الاستبدال النوليوفيلي.
يمكن ان يكون تفضيل الحذف المضاد قوية جداً، كما سنرى في دراستنا للمركبات الحلقية إلا أنه ، وكما سنرى ايضاً، يمكن لتفاعلات E2 في ظروف معينة ان تحدث وفق الحذف المناضد. ومهما يكن من امر، فإن الجزيئات تفعل عادة ما هو اسهل بالنسبة لها.
نتوافق الكيمياء الفراغية الملاحظة لتفاعلات الحذف هذه، بشكل كلي، مع الآلية (E2). تشير درجة الانتقائية الفراغية العالية إلى تفضيل قوي لعلاقة فراغية خاصة بين الزمرتين الراحلتين – إنه امر مفهوم تماماً إنهما ترحلان بشكل متوافق.
يستخدم الكيميائيون "ارترو" و "تريو"، بشكل شائع، للتمييز بين بعض المماكبات اللامتخايلة الحاوية كربونين كيراليين انها مشتقة من أسماء الالدوزات (aldoses) اللامتخايلة الايرتوز والتريوز. إذا رسمنا الصيغ المتصالبة لهذه الالدوزرات بحيث نكون الزمر الاكبر، في الأعلى وفي الأسفل، وتكون الهيدروجينات والهيدروكسيلات متوضعة في كلا الجانبين، نرى من الاريتروز، ان المبادلات المتشابهة (لقلن الهيدروجين) تتوضع في الجهة نفسها من الصيغة، وفي التريوز نكون متوضعة في جهتين متعاكستين.
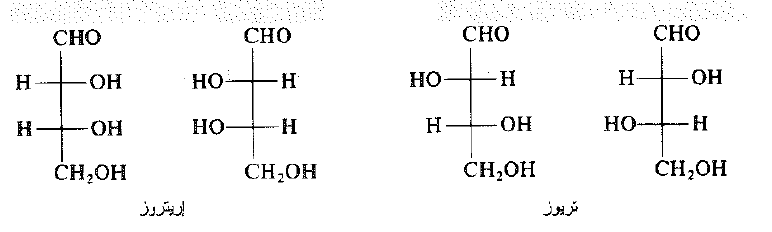
وبالأسلوب نفسه تكون الهيدروجينات في المركب -1 برومو 1- ، 2 – ثنائي فنيل البروبان متوضعة على الجانب نفسه وتكون زمر النيل الكبيرة الحجم في الاعلى والأسفل وذلك في المتماكبات "اريترو"، وفي جهتين متعاكستين في المتماكبات "تريو". (لمساعدتك نذكر ان : في" الاريترو" تكون القضبان الافقية في ذات الجهة، وفي "التريو" تكون في جهتين متعاكستين).