

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الهدركسلة . تشكل الديولات 1- ، 2 Hydrxylation. Formation of 1, 2- diols
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 375
3-4-2017
4510
الهدركسلة . تشكل الديولات 1- ، 2 Hydrxylation. Formation of 1, 2- diols
تحول بعض الكواشف المؤكسدة الالكنات إلى ديولات 1- ، 2 ، أي كحولات ثنائية الهيدروكسي تحتوي على زمرتي –OH عند كربونيين متجاورين (تعرف ايضاً بالغليكولات). يعادل التفاعل إضافة زمرتي هيدروكسيل إلى الرابطة المزدوجة.
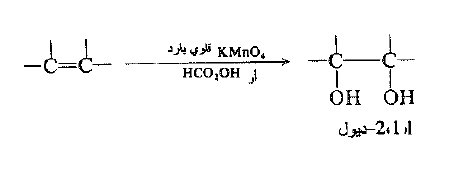
نستخدم عموماً وفي معظم الأحيان من بين الكواشف المؤكسدة المتعددة التي تحدث الهدركسلة (أ) محلولاً قلوباً بارداً من برمنغنات البوتاسيوم، (ب) فوق الحموض مثل فوق حمض الفورميل (HCO2OH)).
ونظراً لكون البرمنغنات احد أهم الكواشف المؤكسدة في الكيمياء العضوية، فإنه من المفروض ان نطلق الآن على بعض صفاتها العامة المميزة. البرمنغنات كاشف مؤكسد قوي، ونختار عند العمل بها الشروط بجذر – الحموضة، القلوية، درجة الحرارة، كمية الكاشف المستخدمة – لتجنب عملية فوق الاكسدة التي تتعدى مرحلة تفاعل الاكسدة الذي نرغب فيه. والمشكلة الرئيسية التي تصادف هي الذوبانية، إذ على المرء في معظم الاحيان أن يجعل البرمنغنات الذوابة في الماء على تماء مع الركيزة غير الذوابة في الماء، زد على ذلك ان كثيراً من المذيبات المستخدمة عموماً لجمع الكواشف القطبية وغير القطبية بعضها مع بعض – الكحولات مثلاً – هي نفسها تتأكسد بالبرمنغنات . وقد حلت هذه الكواشف جزئياً في الوقت الحاضر باستخدام حفازات انتقال الطور يمكن لأيونات الامونيوم الرابعية ان تقل ايونات البرمنغنات من الطبقة المالية إلى الطبقة اللامائية (لنقل البنزين وثنائي كلوريد الايتان) حيث تكمن الركيزة ، ويمكن للأنيرات الناحية أن تشكل معقداً مع أيونات البوتاسيوم وبالتالي تجعل البرمنغنات الصعبة ذوابه في البنزين ، ويكون المنتج هو "البنزين الارجواني" الكاشف المؤكسد الممتاز.
تحصل الهدركسلة بالبرمنغنات بتحريك الألكن في درجة حرارة الغرفة ومحلول البرمنغنات المائي معاً . والمحلول يمكن أن يكون معتدلاً - فينتج التفاعل - - OH، ومن الأفضل أن يكون خفيف القلوية. ونحصل في بعض الأحيان على مردود أعلى باستخدام محاليل "البنزين الارجواني". اهم ما يجب اخذه بالحسبان هو ان تكون الشروط اللازمة غير شديدة. ونتجنب الحرارة وإضافة الحمض، لأن مثل هذه الشروط الأكثر عنقاً تعزز الاكسدة اللاحقة للديولات المترافقة بتشطر الرابطة المزدوجة كربون – كربون.
تحدث الهدركسلة بفوق حمض الفورميك بترك الالكن على تماس مع مزيج من بيروكسيد الهيدروجين وحمض الفورميك HCOOH عدة ساعات. نستخن المنتج بعدئذ من الماء لحلمهة المركبات المتوسطة.
فمثلاً :
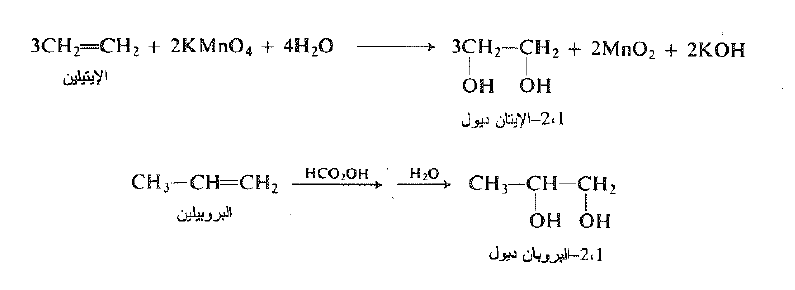
تعد هدركسلة الالكنات من الطرائق الاكثر اهمية في اصطناع الديولات – 1 ، 2 وتتميز بصورة خاصة بالمقدرة على التحكم الكيميائي الفراغي ، عن طريق اختيار الكاشف المناسب.
تكون الاكسدة بالبرمنغنات الأساس الذي يستند إليه اختبار تحليلي مفيد جداً يعرف باختبار باير Baeyer