

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
الاستقرارات النسبية للكربوكاتيونات
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 211 - 6th ed
14-2-2017
996
الاستقرارات النسبية للكربوكاتيونات :Relative stabilities of carbocations
عندما رغبنا في مقارنة استقرارات الجذور الحرة استخدمنا طاقات التفارق اللامتجانس للروابط ، حيث ان هذه تطبق على تفاعلات تتكون فيها الجذور الحرة.
والآن نريد مقارنة استقرارات الكربوكاتيونات، ولكي نفعل سوف تتبع نفس الاسلوب المنطقي الذي اتبعناه مع الجذور الحرة. غير أننا سنبدأ هذه المرة ، بطاقات التفارق اللامتجانس للروابط الواردة في الجدول 3.1 ، لأنها تطبق على تفاعلات تتكون فيها الكربوكاتيونات. نجد في هذا الجدول طاقات الروابط التي تصل البروم إلى عدد من الزمر.
هذه قيم ….. للتفاعلات التالية:
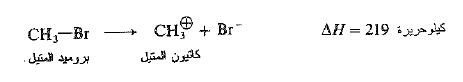
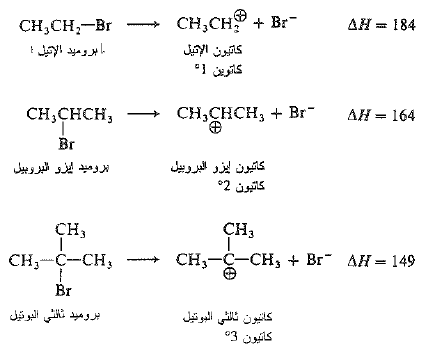
وبالتعريف فإن طاقة التفارق هذه، هي كمية الطاقة الواجب تقديمها لتحويل مول من بروميد الكيل إلى كربوكاتيونات وأيونات بروميد.
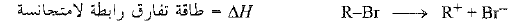
وكما نرى فإن كمية الطاقة اللازمة لتكوين مختلف صنوف الكربوكاتيونات تتناقص وفق الترتيب:
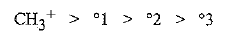
إذا لزمت طاقة أقل لتشكيل كربوكاتيون ما من الطاقة اللازمة لتشكيل كربوكاتيون آخر، فإن هذا يعني فقط، أن أحد الكربوكاتيونات يحوي طاقة أقل من الآخر، نسبة إلى بروميد الألكيل الذي تكون منه، وبكلمات أخرى، فإن احدهما اكثر استقراراً من الآخر (انظر الشكل 1.1).
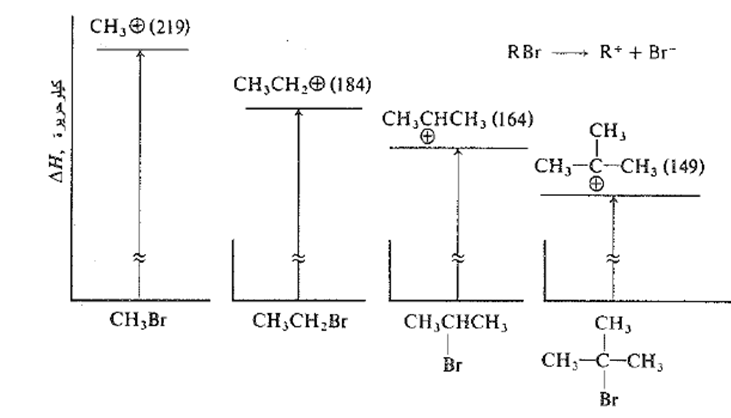
الشكل 1.1 : استقرارات الكاربوكاتيونات بالنسبة لبروميدات الالكيل الموافقة ( رتبت المخططات بمايوافق بعضها البعض لتسهيل المقارنة)
نحن لا نحاول مقارنة الحتوى الطاقي في المطلق، لكاتيونات ايزو البروبيل وثالثي البوتيل مثلاً ، إننا نقول ببساطة ان الفرق في الطاقة بين البروبيل وكاتيون ايزو البروبيل هو اكبر من فرق الطاقة بين بروميد ثالثي البوتيل وكاتيون ثالثي البوتيل. إذن عندما نقارن استقرارات الكربوكاتيونات، فإنه يجب ان يكون مفهوماً ان معيارنا لكل كاتيون، هو الركيزة التي تكون منها الكربوكاتيون. وكما سنرى، هذا هو بدقة نوع الاستقرار الذي يعنينا.
استدمنا فيما سبق بروميدات الكيل للمقارنة ، غير انه يمكننا ان نستخدم بشكل جيد فلوريدات الكبل وكلوريدات الكيل ويوديدات الكيل، أو الكحولات الموافقة. تظهر طاقات تفارق الروابط في الجدول 3.1، من اجل جميع هذه المركبات، الترتيب نفسه في استقرار الكربوكاتيونات. وحتى حجوم الفروق في الطاقة بين كاتيون المتيل وثالثي البوتيل، منسوباً إلى ركائزها كما يلي: الفلوريدات 67 كيلو حريرة، والكلوريدات 70 كيلور حريرة، والبروميدات 70 كيلو حريرة، واليوديدات 72 كيلو حريرة والكحولات 66 كيلو حريرة.
ويكون ترتيب استقرار الكربوكاتيونات ، نسبة إلى الركائز التي منها تكونت ، هو استقرار الكربوكاتيونات 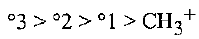
سوف نرى ان هذا الترتيب لا يطبق، فقط عندما تتكون الكربوكاتيونات بالتحلل غير المتجانس، بل وكذلك عندما تتكون بطرائق مختلفة كلياً.
ان الفروق في الاستقرار بين الكربوكاتيونات اكبر بكثير من تلك التي بين الجذور الحرة. فمثلاً، يكون جذر ثالثي البوتيل اكثر استقراراً بمقدار 12 كيلور حريرة فقط، من جذر المتيل، بينما يكون كاتيون ثالثي البوتيل، تبعاً للركيزة المتكون منها، اكثر استقراراً بمقدار 72-66 كيلو حريرة من كاتيون المتيل. وكما سنرى ، فإن هذه الفروقات الكبيرة في الاستقرار تؤدي إلى زيادات كبيرة في التأثيرات في التفاعلية.
بني نقاشنا حتى الآن في هذه الفقرة على طاقات تفارق الروابط، التي قيست في الطور الغازي . وكما نعلم، فإن جميع كيمياء الكربوكاتيون تقريباً، تجري في محاليل، وتستطيع المذيبات ان تمارس دوراً قوياً في التأثير على المواد المذابة الايونية. هل اعطي ترتيب الاستقرار للكربوكاتيونات الذي توصلنا إليه، في محلول ؟ أعطيت الإجابة على هذا السؤال مباشرة بقياس قيم … ، في مذيبات متنوعة ، لحيل من الكربوكاتيونات بطريقة أولاه Olah الحمضية.

أظهرت القيم المقاسة نفس ترتيب استقرار الكربوكاتيون منسوباً إلى الركيزة الوالدة، الذي أظهرته طاقات التفارق. وحتى الفروقات في الاستقرار مقاسة بالكيلو حريرة/ مول، تتبع الامر ذاته .
وهكذا توصلنا إلى ترتيب استقرار الكربونكاتيونات الذي يبديه في المحاليل تماماً، كما يبديه في الطور الغازي، كيميائية واسعة التنوع. سوف نضيف، أثناء متابعتنا لدراستنا، أنواعاً اخرى من الكربوكاتيونات إلى سلاسل ترتيباتنا، ونتفحص أنواعاً اخرى من التفاعلات التي يمكن ان تتكون بوساطتها هذه الكربوكاتيونات.
لنر الآن كيف يمكن أن يفسر ترتيب الاستقرار هذا.