

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
المدارات الهجينة: sp2 Hybrid orbitals: sp2
المؤلف:
Robert T. Morrison & Robert. N Boy
المصدر:
الكيمياء العضوية Organic chemistry
الجزء والصفحة:
p 13 - 6th ed
31-10-2016
3282
المدارات الهجينة: sp2 Hybrid orbitals: sp2
لندرس جزيء ثلاثي فلوريد اليور BF3. يملك البور الكتروناً واحداً غير متزاوج، يشغل أحد المدارات 2p. نحتاج لتكوين ثلاث روابط، ثلاثة الكترونات غير متزاوجة، ولذلك نرفع الكتروناً واحداً 2s الى أحد
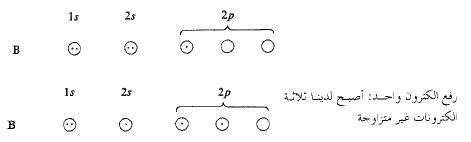
إذا كان مطلوباً منا هذه المرة أن ننشئ الجزيء الأكثر استقراراً، فإنه مطلوب بناء روابط أكثر قوة ولتحقيق ذلك علينا توفير المدارات الذرية التي لها قوة موجهة أشد ما يمكن. ومرة أخرى نجد أن التهجين يوفر مثل هذه المدارات: ثلاثة مدارات هجينة مكافئة تماماً بعضها لبعض ولكل منها الهيئة المبينة في (الشكل 7.1)؛ وكما سبق، سنهمل الانتفاخ الصغير الخلفي ونمثل الأمامي على شكل كرة.
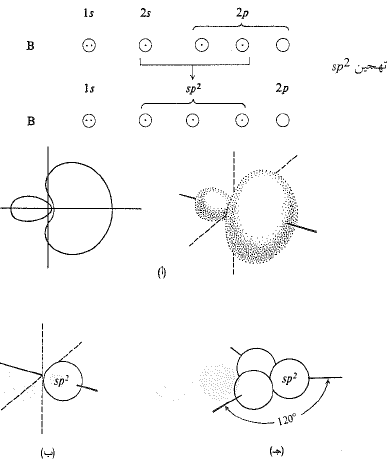
الشكل 1.1: مدارات هجينة sp2. (أ) مقطع عرضي والهيئة التقريبية لمدار مفرد، موجه بقوة وفق محور واحد. (ب) تمثيل بشكل كرة، مع حذف الانتفاخ الخلفي الصغير. (جـ) ثلاثة مدارات ذات محاور موجهة نحو رؤوس مثلث متساوي الأضلاع.
تدعى هذه المدارات الهجينة، المدارات sp2، لأنها تعد ناتجة من مزج مدار واحد s مع مدارين اثنين p. تتوضع هذه المدارات في المستوى الذي يحوي نوى الذرات، وتتجه نحو رؤوس مثلث متساوي الأضلاع؛ وتكون قيمة
الزاوية بين أي مدارين مساوية 120˚. ومرة ثانية نرى أنفسنا هنا أمام هندسة تسمح للمدارات بأن تتخذ وضع تكون فيه أبعد ما يمكن بعضها عن بعض؛ هذا الوضع هنا هو الوضع المثلثي (ثلاثي الزوايا) وعندما نرتب الذرات بحيث نحقق التراكب الأعظم لكل مدار من المدارات sp2 التابعة للبور مع مدار p للفلور، نحصل على البنية الموضحة في الشكل 8.1. أي نحصل على جزيء مستو تحت فيه ذرة البور مركز المثلث المتساوي الأضلاع، في حين تقع ذرات الفلور في رؤوسه. وتكون الزاوية بين كل رابطتين مساوية 120˚.
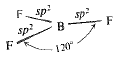
الشكل 8.1: جزيء BF3
لقد بينت التجربة أن ثلاثي فلوريد البور له بالفعل هذه البنية المتناظرة التي حسبت بواسطة ميكانيك الكم.