

علم الكيمياء

تاريخ الكيمياء والعلماء المشاهير

التحاضير والتجارب الكيميائية

المخاطر والوقاية في الكيمياء

اخرى

مقالات متنوعة في علم الكيمياء

كيمياء عامة


الكيمياء التحليلية

مواضيع عامة في الكيمياء التحليلية

التحليل النوعي والكمي

التحليل الآلي (الطيفي)

طرق الفصل والتنقية


الكيمياء الحياتية

مواضيع عامة في الكيمياء الحياتية

الكاربوهيدرات

الاحماض الامينية والبروتينات

الانزيمات

الدهون

الاحماض النووية

الفيتامينات والمرافقات الانزيمية

الهرمونات


الكيمياء العضوية

مواضيع عامة في الكيمياء العضوية

الهايدروكاربونات

المركبات الوسطية وميكانيكيات التفاعلات العضوية

التشخيص العضوي

تجارب وتفاعلات في الكيمياء العضوية


الكيمياء الفيزيائية

مواضيع عامة في الكيمياء الفيزيائية

الكيمياء الحرارية

حركية التفاعلات الكيميائية

الكيمياء الكهربائية


الكيمياء اللاعضوية

مواضيع عامة في الكيمياء اللاعضوية

الجدول الدوري وخواص العناصر

نظريات التآصر الكيميائي

كيمياء العناصر الانتقالية ومركباتها المعقدة


مواضيع اخرى في الكيمياء

كيمياء النانو

الكيمياء السريرية

الكيمياء الطبية والدوائية

كيمياء الاغذية والنواتج الطبيعية

الكيمياء الجنائية


الكيمياء الصناعية

البترو كيمياويات

الكيمياء الخضراء

كيمياء البيئة

كيمياء البوليمرات

مواضيع عامة في الكيمياء الصناعية

الكيمياء الاشعاعية والنووية
صميم الميوجلوبين يؤمن بيئة تحمي حديد الهيم
المؤلف:
د. روبرت موراي وآخرون
المصدر:
هاربرز في الكيمياء الحيوية
الجزء والصفحة:
ص 192
20-5-2021
2727
صميم الميوجلوبين يؤمن بيئة تحمي حديد الهيم
عند ارتباط جزيء الاكسجين بالميوجلوبين تكون الرابطة بين الذرة الأولى للأوكسجين واحديد (+Fe2) متعامدة مع مستوي حلقة الهيم، أما الاكسجين التالي فيرتبط بزاوية 121 درجة مئوية مع مستوي الهيم ويتوجه بعيدا عن الهيستيدين القاصي (الشكل 7-5).
يرتبط أول أكسيد الكربون (CO) مع الهيم الحر بشكل أقوى بنحو 25,000 مرة مما يفعل بالاكسجين. ويحتوي الجو المحيط على أثار من CO، كما ينجم عن التقويض الطبيعي للهيم نفسه كميات صغيرة من CO؛ فلماذا إذاً لا يشغل CO (وليس O2) موضع التشارك السادس من حديد هيم الميوجلويين؟ يكمن السبب في الإعاقة التي يقوم بها صميم الميوجلوبين حول الهيم، فالتوجه المفضل لارتباط CO بحديد الهيم هو أن تكون الرابطة بين الذرات الثلاث (O ،C ،Fe) عمودية على حلقة الهيم (الشكل 7-5). وفي حين يكون هذا التوجه ممكنا بالنسبة إلى الهيم الحر، يعمل الهيستيدين القاصي في الميوجلوبين على الإعاقة الفراغية لارتباط CO بهذه الزاوية (الشكل 7-6)، وهذا ما يجبر على أن يرتبط CO بشكل فراغي أقل استقرارا ويخفف من قوة الارتباط بين الهيم و CO بأكثر من الضعفين (إلى حوالي 200 مرة من قوة الارتباط بين الهيم و O2). وعلى العموم، يوجد جزء صغير من الميوجلوبين الطبيعي (نحو 1 %) بشكل أول أكسيد كربون الميوجلوبين.
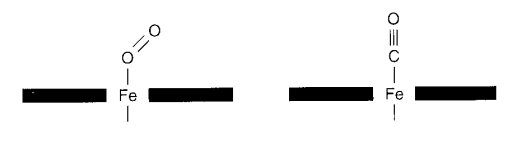
الشكل 7-5 : الزوايا المفضلة لارتباط الأكسجين وأول أكسيد الكربون إلى ذرة حديد الهيم (الخط الغامق).
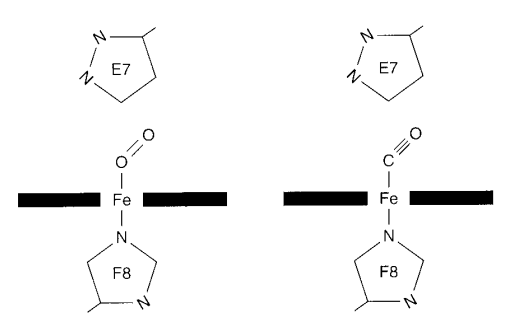
الشكل 7-6 : زوايا ارتباط الأكسجين وأول أكسيد الكربون إلى حديد هيم الميوجلوبين. يعيق الهيستيدين البعيد E7 ارتباط CO بزاويته اسئلة 180 (م) نسبة إلى مستوى حلقة الهيم.